兔急性视网膜坏死模型的建立及对侧眼发病途径的探讨
作者单位:100730 首都医科大学附属北京同仁医院眼科中心;北京市眼科学与视觉科学重点实验室
【摘要】目的 建立兔急性视网膜坏死模型并探讨该病对侧眼发病的感染途径。设计 实验性研究。研究对象41只成年青紫蓝兔。方法 经睫状体扁平部将单纯疱疹病毒(HSV-1)注射于兔视乳头旁的视网膜下,建立急性视网膜坏死(ARN)动物模型。在注射病毒后1、3 天开始对模型动物分别用更昔洛韦玻璃体腔注射、静脉注射以及玻璃体腔注射联合静脉注射三种方式治疗。通过PCR方法检测血液中是否存在病毒。部分动物做眼球和脑组织病理检查。主要指标血液的PCR病毒学检测结果,眼球、视神经、脑组织的病理改变。结果10只兔在接种病毒后10~18天双眼先后发生ARN,15只兔出现神经系统损害。双眼发病的动物中,5只兔在对侧眼发病前后(病毒注射后 9~19 天),血液PCR中均未检测到病毒存在。眼球、视神经、脑组织均有淋巴细胞和浆细胞浸润。结论 可于兔视网膜下注射HSV-1建立ARN模型。在兔ARN模型中双眼病变者未发现病毒通过血液感染的征象,是否经视神经途径感染有待进一步研究。
【关键词】视网膜坏死;动物模型
在人类急性视网膜坏死(acute retinal necrosis,ARN)中,大约有1/3病例为双眼先后发病[1]。至今,双眼发病的原因还没有明确结论。Freeman等[2]将单纯疱疹病毒(HSV-1型、PH株)通过睫状体平部注射于青紫蓝兔视网膜下,成功建立了亚急性视网膜坏死的动物模型,之后在此模型基础上进行了一系列关于长效抗病毒药物的研究。在这些模型动物中,也有双眼发病的情况。
HSV-1型KOS株病毒是临床分离所得,有很强的致病性。本文借鉴Freeman的方法,以此病毒感染青紫兰兔,也成功地建立了视网膜坏死的动物模型。在这些实验动物中,也有一些表现为双眼发病。 因此想从动物模型的角度对ARN对侧眼发病的机理进行探讨。
材料和方法
一、材料
研究材料包括青紫蓝兔41只,体重 2~2.5kg;通过肾肿瘤细胞(VERO细胞)扩增的单纯疱疹病毒1型(HSV-1,KOS 株),滴度为 4.25×106个病毒颗粒/ml;更昔洛韦粉剂50mg/支;氟美松注射液(5mg/ml) 全自动荧光PCR 分析仪 HSV-1 PCR荧光检测试剂盒。
二、方法
1.ARN动物模型的制备:动物以复方托吡卡胺滴眼液散瞳后以地西泮2ml(10mg/L)、盐酸氯胺酮2ml(0.1g/L)后肢肌肉注射麻醉。将胰岛素注射器针尖适当弯曲后,抽取0.08ml(34000个病毒颗粒)病毒液,于角膜缘后2mm倾斜刺入巩膜板层少许, 后垂直刺入玻璃体腔(防止玻璃体注射时液体返流),在显微镜下于视盘旁有髓神经纤维处轻柔地刺入视网膜下,再稍向前潜行,将病毒注入视网膜下。出针后前房穿刺降低眼压。
2.动物模型的药物治疗:兔眼的玻璃体腔容积是人眼的0.4倍,依照人体玻璃体注射更昔洛韦(GCV)的最大用量2000μg[3]计算,实验中的GCV玻璃体注射量为800μg。治疗人眼内炎时玻璃体注 射氟美松的用量为200~400μg, 用最大剂量的0.4倍即氟美松160μg作玻璃体联合注射。GCV耳缘静脉注射用量依照人体用量标准5mg/kg体重计算。治疗起始时间为动物接种病毒后24小时(定为感染早期)以及72小时(定为感染晚期)。GCV以乳酸林格液溶化。
①玻璃体注药组:角膜缘后2mm向玻璃体内注入GCV。首次注药后7天再重复注药一次。
②静脉注射组:从耳缘静脉缓慢注射GCV,每天2次,间隔6小时,持续14天。
③玻璃体注射—静脉注射联合治疗组:药物剂量同前两组,间隔7天玻璃体注射2次,静脉注射每天2次,持续14天。
④GCV 联合氟美松玻璃体注药组:氟美松 与 GCV 同时注入玻璃体,首次注药后7天再重复注药一次。
3. 视网膜病变分级及药物疗效的判定:术后每天观察双眼前节及眼底,部分动物照眼底像,并注意全身情况。根据 Freeman 等[2]和 Beson 等[4]的动物模型视网膜病变分级标准观察和记录分级。药物治疗效果的判定,以眼底病变的分级高低为标准,分级越高,疗效越差。结果以SPSS统计软件作秩和检验。
视网膜坏死模型分级0级:视盘充血、水肿;1级:视盘片状出血,有髓纤维片状出血、有细小的病灶玻璃体轻度混浊,有膜状漂浮物 2级:下方视网膜散在的局限性病灶,1个象限受累3级:下方视网膜病变融合,玻璃体混浊加重,有片状、球状混浊2个象限受累;4级:超过2/3面积的视网膜有片状病灶玻璃体混浊加重。
4.病原学PCR分析:在模型和治疗的每个阶段的不同时间从兔耳缘静脉取血,用荧光定量PCR的方法做HSV-1病原检查,以判断血液中是否存在病毒。作为对照,病毒接种液、接种眼的视网膜和脉络膜组织、未接种动物的血液均做了相同的PCR检测。
5.病理分析:每组动物观察结束后耳缘静脉注射空气处死取眼球、脑组织送常规病理切片、HE染色,观察组织的病变情况。
结 果
一、原始动物模型的表现
视网膜下接种病毒时,产生医原性局限视网膜脱离。2天后视网膜复位。术后玻璃体清亮。术后 2~3天,视盘开始充血,水肿,后极部有沿血管走行的羽毛状视网膜出血。视网膜病灶起初为淡白色边界比较清晰的圆形或条形薄棉絮样混浊,出现在下半视网膜后极部和周边部。并且伴有渗出性视网膜 脱离。第4天病灶开始融合后极部小病灶可保持独立、分散而周边病灶则倾向于融合。第8~10天病灶有“收缩”的倾向,边缘开始变得更加清晰,颜色更苍白而浓厚。同时玻璃体混浊和视乳头水肿减轻,并开始出现视网膜裂孔。第14~18天裂孔扩大,视网膜脱离、变薄、乃至破碎。残留视网膜有如纱膜,透过视网膜缺损区可以清晰地看见脉络膜。全视网膜脱离时,血管呈“V”字形悬浮于玻璃体。本组模型中视网膜病变都达到3级和4级(图1~4)。

二、药物治疗后的眼底病变分级
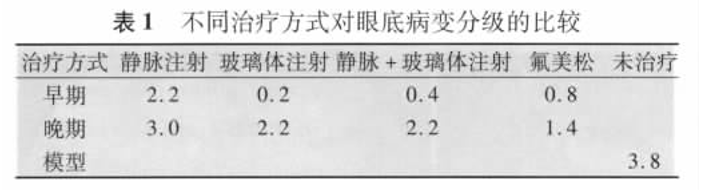
根据治疗后眼底病变的分级(表1)可以看出,在早期治疗中玻璃体注射、玻璃体+静脉联合注射比单纯静脉注射疗效好玻璃体注射与联合注射疗效近似。在晚期治疗中,各种给药方式之间疗效没有明显差异。
三、对侧眼的表现和神经系统症状的表现
在这些动物中,共有10只兔双眼发病,其中治疗阶段有7只。对侧眼早期表现为视盘充血瞳孔对光反射消失。随后视网膜出现病灶为周边开始 的均匀分布的白点累及全视网膜3~4天即可出现后极部视网膜脱离、视网膜裂孔,脱离后的视网膜有如纱膜。出现神经系统症状者15只其中治疗阶段9只5只为双眼发病其中治疗阶段有4只。中枢症状表现为眼球震颤、咀嚼肌痉挛、站立不稳、角弓反张、不进食水,发病2~3天死亡。
四、病毒学PCR检测结果
5只兔做了血液HSV-1的PCR病毒学检测。2只取血时间在对侧眼发病之前3只在之后(表2)。血液PCR检测病毒结果均为阴性。作为对照的标本结果是:未接种病毒的动物血液PCR阴性;接种眼视网膜、脉络膜PCR阳性病毒接种液PCR阳性。
五、病理结果
标准动物模型的典型病理表现为病毒接种眼的视网膜水肿、疏松、萎缩,内外核层分界模糊、细胞空泡变淋巴细胞、浆细胞浸润。色素上皮层和视细胞连续性中断、细胞崩解脱失。脉络膜增厚、淋巴细胞、浆细胞浸润。玻璃体内有不均匀的纤维素样渗出、出血和淋巴细胞、浆细胞浸润偶见中性多型核细胞。视盘有大量淋巴细胞、浆细胞浸润,有灶状坏死,血管周围有“套袖征”。视神经疏松、空泡变、萎缩淋巴细胞、浆细胞浸润(图5,6)。
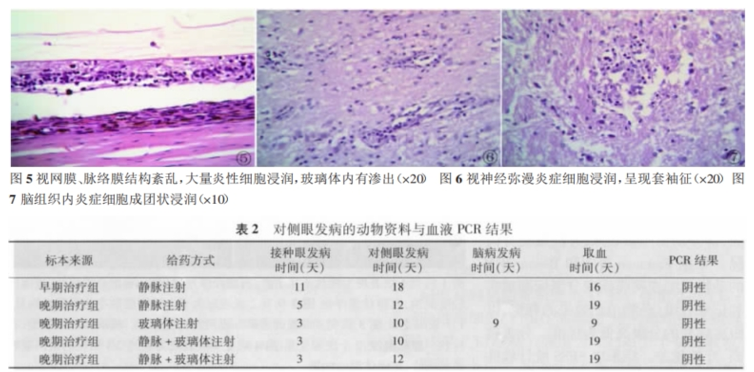
治疗后各实验组眼底炎症分级不同,但眼底病理表现都有与动物模型部分相同的坏死表现,只是视网膜组织的破坏程度、炎症细胞的浸润程度有所减轻。
对侧眼发病的眼底表现轻重不同,眼底病变明显者,病理同模型眼的典型表现。病变轻者病理为轻 度的视网膜结构紊乱、少量淋巴细胞、浆细胞浸润。
脑组织:有神经系统症状者可见脑组织皮质、皮质下均有神经细胞坏死,大量淋巴细胞、浆细胞浸润,伴有少量嗜酸细胞、中性多形核细胞,大量小胶质细胞增生。血管充血扩张,四周淋巴细胞浸润,成“套袖”样(图7)。
双眼发病动物的视神经:双侧视神经都有类似脑组织感染的表现,且轻重程度与双眼病变的程度相一致。
讨 论
可依据Freeman的方法建立兔眼ARN模型,但ARN的发病机理尚不清楚,多认为是病毒感染后继发免疫性损害。有大约1/3的病例在第一只眼发病后1至3个月对侧眼也发病[1],对侧眼发病的机制也不明确。
目前有逆行感染的学说[5,6]。有报道患有HSV脑炎的患者行开颅手术后双眼发生ARN[7],推测中枢神经系统的病毒在手术中受到刺激而激活,经由视交叉、视神经感染到双侧视网膜,即病毒经神经轴索由中枢向眼部逆行感染。病毒被激活的原因可能还包括全身大量应用糖皮质激素。还有研究者用带有标记物的HSV-1 RH116株接种于鼠前房,在对侧眼可以产生典型的ARN模型,而接种眼不会发病[6,8]。追踪病毒的感染途径发现,病毒是经过动眼神经的副交感纤维到达脑干的EW核,然后在双侧中枢神经核团扩散,再经过对侧眼的视神经到达对侧视网膜神经节细胞、内核层,最后感染感光细胞,引起视网膜坏死。表明此模型对侧眼的病变是病毒由中枢向眼部逆行感染的结果。本研究中病毒直接接种于眼底,而不是前房;接种眼本身有坏死。因此上述结论不能解释本实验的结果。
ARN多见于身体健康者,即使对侧眼发病也没有特定的中枢神经系统症状。在动物模型中,双眼发病者有部分脑病表现。本实验中双眼发病者10只,伴有角弓反张等外在脑病表现者5只。在Freeman的模型中,双眼发病者,病理发现40%没有脑炎,20%为单侧脑炎,40%为双侧脑炎。由此看见,对侧眼发病不是必然发生在脑部感染之后,接种眼的病毒不一定是从接种眼经过中枢逆行感染而来。
是否有血行感染的可能性呢? PCR 技术已经广 泛应用于病原体的检测,是一种灵敏高效的检测手 段。可以检测既往感染、现症感染,并能够克服免疫 学检测的“ 窗口期”。考虑到病毒接种之后需要一定 的时间复制,采集血样的时间选择了接种眼出现病变之后。即表明已经有大量病毒复制,具备了出现病毒血症条件的时候。同时又包括了对侧眼出现病变之前和之后的时间范围。但是PCR结果均为阴性,没有发现病毒经过血液传播的证据。
还有一种可能性,即病毒由一侧眼经过视神经到视交叉、到对侧视神经、再到对侧眼的感染途径。从视神经的纤维走行来看,双侧眼在视交叉并没有直接的传导通路,但是有物理上的接触。更明确的结论需要待跟踪了带标记物的病毒感染途径后才能获得。
总之,ARN双眼发病的机理还不完全清楚,血液标本的PCR结果不支持病毒经血行感染的传播方式。病毒示踪的方法有可能揭示真正的原因。
参考 文 献
[1]Gartry DS,Spalton DJ,Tilzey A,et al.Acute retinal necrosis syndrome. Br J Ophthalmol,1991,75:292-297.
[2]Freeman WR,Schneiderman TE,Wiley CA,et al. An animal model of focal,subacute,viral retinitis. Retina,1993,13:214-221.
[3]Schulman J,Peyman GA,Horton MB,et al.Intraocular 9-([2-hydroxy-1-(hydroxymethyl)ethoxy]methyl)guanine levels after in-travitreal and subconjunctival administration. Ophthalmic Surg,1986,17:429-432.
[4]Besen G,Flores-Aguilar M,Assil KK,et al.Long-term therapy for herpes retinitis in an animal model with high-concentrated lipo-some-encapsulated HPMPC.Arch Ophthalmol, 1995,113:661-668.
[5]Tanigawa M,Bigger JE,Kanter MY,et al. Natural killer cells prevent direct anterior-to-posterior spread of herpes simplex virus type 1 in the eye. Invest Ophthalmol Vis Sci,2000,41:132-137.
[6]Tornerup NR,Fomsgaard A,Nielsen NV.HSV-1-induced acute retinal necrosis syndrome presenting with severe inflammatory or-bitopathy,proptosis,and optic nerve involvement.Ophthalmology,2000,107:397-401.
[7]Perry JD,Girkin CA,Miller NR,et al. Herpes simplex encephalitis and bilateral acute retinal necrosis syndrome after craniotomy. Am J Ophthalmol,1998,126:456-460.
[8]Pendergast SD,Werner J, Drevon A,et al. Absence of herpesvirus DNA by polymerase chain reaction in ocular fluids obtained from immunocompetent patients.Retina,2000,20: 389-393.
-
BMC瑞迈特新品获iF设计奖,创新设计助力基层睡眠呼吸筛查
2026-03-26 10:41:03
-
依视路陆逊梯卡亮相上海眼镜展 共筑价值驱动的眼健康新生态
2026-03-04 10:53:24
-
我国首个支气管镜机器人肺结节治疗领域专家共识正式发布,填补国内空白
2025-06-18 18:22:04
MedTrend
∣ 医趋势
医疗前沿资讯 | 趋势观察洞见 | 组织与领导力 | 人才解决方案


长按,识别二维码,加关注
